针对骨髓脂肪细胞预防骨质流失的新机制
骨髓脂肪细胞 (BMAd) 位于骨微环境中,紧邻骨细胞、血管结构和造血组织。由于病理生理条件导致骨微环境中信号异常,骨髓基质/干细胞 (BMSCs) 谱系向定向脂肪形成祖细胞转变,而骨祖细胞减少。
然而,过量 BMAd(特别是在病理生理条件下)介导骨驻留细胞之间细胞通讯的确切机制仍不清楚。
近日,中国科学院深圳先进技术研究院管敏研究员团队发现,脂肪细胞中雌激素相关受体α(ESRRA)缺失,导致分泌因子表达发生改变,对骨髓间充质干细胞命运决定和血管内皮细胞血管生成有协同作用,提示靶向脂肪细胞中的ESRRA可能成为骨质疏松症的潜在治疗靶点。
该研究于 5 月 4 日发表在《自然通讯》上。
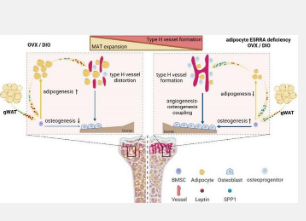
在本研究中,研究人员发现脂肪细胞特异性的 ESRRA 敲除可挽救骨质流失和 H 型血管扭曲,并抑制卵巢切除术 (OVX) 或饮食引起的肥胖 (DIO) 引起的小鼠骨髓脂肪沉积。
实验结果表明,脂肪细胞ESRRA干扰17-雌二醇和雌激素受体α的信号传导,导致分泌性磷蛋白1(Spp1)的转录抑制。因此,ESRRA缺陷的脂肪细胞释放SPP1可增强内皮细胞迁移,并恢复OVX或DIO诱导的小鼠的H型血管形成。
此外,ESRRA 通过与瘦素启动子结合,积极调节瘦素表达。因此,ESRRA 的消除会降低内脏脂肪细胞和 BMAd 的瘦素分泌,促使 BMSC 分化为成骨细胞而不是脂肪细胞。
此外,药理学抑制 ESRRA 可显著限制骨髓脂肪组织扩张,促进肥胖小鼠富含脂肪细胞的骨环境中的骨形成,从而防止骨质流失和高骨髓脂肪沉积。
该研究通过针对ESRRA为治疗骨骼疾病,特别是与高骨髓脂肪沉积相关的临床病症提供了一种新方法。
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
