用于增强CART细胞治疗的淋巴结样生物材料支架
由浙江大学药学院顾震博士和李红军博士以及浙江大学医学院孙杰博士领导的研究小组旨在提高CAR-T细胞疗法的治疗效果用于实体瘤。虽然在治疗 B 细胞相关白血病、淋巴瘤和多发性骨髓瘤方面表现出有效性,但当前 CAR-T 疗法在实体瘤中面临着挑战,其特点是细胞浸润不足、CAR-T 在肿瘤内的持久性有限,以及阻碍其活性的不利微环境。
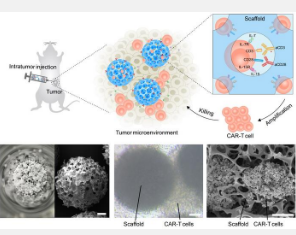
“承认淋巴结作为免疫系统的重要组成部分的关键作用,负责 T 细胞的招募、容纳和激活。我们认为,制造模仿淋巴结结构和功能的人工支架可能会导致“细胞工厂”的发展。这种设想的细胞工厂在注射到肿瘤部位后,有可能显着促进支架内预装 CAR-T 细胞的原位激活和增殖。”李红军博士说。
利用微流体技术,研究人员构建了一种基于聚乳酸-乙醇酸(PLGA)的多孔微球支架。评估显示平均支架直径和孔径分别为 570 μm 和 25 μm,每个球体可容纳约 38,000 个 CAR-T 细胞。该研究的第一作者 Ziyan Liao 强调了高负载能力和强大机械性能的重要性,他指出:“支架将 CAR-T 细胞有效递送至实体瘤的能力取决于这些工程设计细节。”
此外,研究小组在支架上装饰了两种 T 细胞激活的关键信号分子——抗 CD3 和抗 CD28 抗体——进一步模拟淋巴结中发现的抗原呈递细胞。在评估 CAR-T 细胞增殖时,他们观察到支架在体外诱导显着的 50 倍扩增,在植入的皮下肿瘤模型中诱导 15 倍的扩增。值得注意的是,即使在这种高度扩张之后,支架刺激的细胞仍保持良好的杀伤活性。孙杰博士表示:“这一点至关重要,因为实体瘤内 CAR-T 细胞活性的减弱是该疗法的一个关键挑战。”研究人员通过在异种移植人宫颈癌小鼠模型中证明通过这种策略传递的 CAR-T 细胞增强的抗肿瘤作用,证实了他们的发现。
“生物材料支架就像一个淋巴结,可以在肿瘤内持续产生 CAR-T 细胞,为增强实体瘤治疗中的 CAR-T 疗法提供了一种新策略。虽然这项工作的重点是 CAR-T 细胞,但该细胞递送平台也可以帮助其他类型的治疗细胞。”顾振博士总结道。
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
